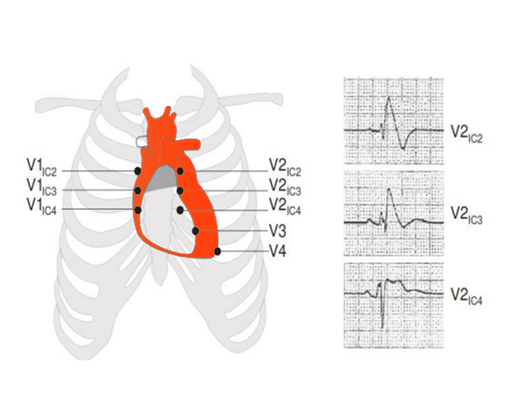
La Sindrome di Brugada è una malattia ereditaria che predispone allo sviluppo di aritmie cardiache maligne e, nella peggiore delle eventualità, alla morte improvvisa. Il cuore di chi ne è affetto è morfologicamente normale, tuttavia , le cellule presentano un “difetto elettrico” che, pur consentendo loro di lavorare in modo apparentemente normale, le espongono al rischio di sviluppare aritmie potenzialmente fatali. È importante sottolineare che le persone affette da questa malattia non hanno i sintomi tipici dei “cardiopatici” (dolori al petto, dispnea , ridotta tolleranza all’ esercizio fisico, ecc.), ma risultano nella stragrande maggioranza dei casi del tutto asintomatici . La categoria a rischio è invece rappresentata da coloro che presentano nel corso della loro vita una perdita di coscienza con rapido recupero dello stato di vigilanza non preceduta da sintomi (sincope cardiogena), un precedente arresto cardiaco rianimato, respiro agonico notturno, crisi morfeiche oppure una storia di familiarità per morte improvvisa, associati ad alterazioni elettrocardiografiche tipiche per pattern di Brugada tipo I.


Abbiamo raccolto i riferimenti di diversi centri italiani e non specializzati nella terapia delle malattie aritmiche ereditarie. L’obiettivo è di aiutare i pazienti affetti da Sindrome di Brugada e le loro famiglie ad entrare in contatto con le strutture mediche specialistiche.
L’elenco non comprende tutti i Centri presenti in Italia e non, ma vuole rappresentare una guida per chi è alla ricerca di una struttura con esperienza in tale ambito a cui rivolgersi.
Universitair Ziekenhuis Brussel - UZ Brussel
Indirizzo: Avenue du Laerbeek, 101, 1090 Jette
Referente: Prof. Carlo De Asmundis
Telefono: +32 24776009
Email: hrmc@uzbrussel.be
Azienda Ospedaliera 'Spedali Civili' di Brescia
Indirizzo: Piazzale Spedali Civili, 1, 25123 Brescia BS
Telefono: 030 3996320
Email: protocollo.spedalicivilibrescia@legalmail.it
Ambulatorio di Cardiologia molecolare - Istituto Maugeri IRCCS Pavia
Indirizzo: Via Salvatore Maugeri, 10, 27100 Pavia PV
Referente: Prof.ssa Silvia G. Priori
Telefono: 0382 592055
Email: cardiologia.molecolare@icsmaugeri.it
Servizio di Elettrofisiologia ed elettrostimolazione
Azienda Ospedaliera Universitaria Sant’Andrea
Indirizzo: Via di Grottarossa, 1035, 00189 Roma RM
Referente: Prof. Pietro Francia
Telefono: 06 33775979
Email: elettrofisiologia@ospedalesantandrea.it
Cardiologia U, Dipartimento Cardiovascolare e Toracico
A.O.U. Città della Salute e della Scienza di Torino
Ospedale Molinette
Indirizzo: Corso Bramante, 88, 10126 Torino TO
Referente: Dott.ssa Carla Giustetto
Telefono: 011 6335319; 011 6335419
UOSA Cardiologia Aritmologia Dipartimento Scienze Cardiovascolari e Toraciche
Università Cattolica del Sacro Cuore
Policlinico Gemelli Roma
Indirizzo: Policlinico Gemelli, 00168 Roma RM
Telefono: Segreteria 06 3015.4187
Ospedale Casa Sollievo della Sofferenza
Cardiologia UTIC
S. Giovanni Rotondo
Indirizzo: Viale Cappuccini, sn, 71013 San Giovanni Rotondo FG
Telefono: 0882 410351
Email: cardiologia@operapadrepio.it
Centro Aritmie Genetiche
Istituto auxologico Italiano San Luca
Indirizzo: Piazzale Brescia, 20, 20149 Milano MI
Referente: Prof.ssa Lia Crotti
Telefono: 0255000.400
Email: centroaritmiegenetiche@auxologico.it
Ambulatorio di Aritmologia, Divisione di Cardiologia
ASST Settelaghi
Ospedale di Circolo-Varese
Indirizzo: Viale Luigi Borri, 57, 21100 Varese VA
Referente: Prof. Roberto de Ponti
Telefono: 0332 278367
Ambulatorio di Aritmologia
Ospedale Papa Giovanni XXIII di Bergamo
Indirizzo: Piazza OMS, 1, 24127 BG
Referente: Dott.ssa Paola Ferrari - Dott. Paolo de Filippo
Email: pferrari@asst-pg23.it
Ambulatorio di Aritmologia e controllo pacemaker e defibrillatori
Centro di Alta Specialità di Elettrofisiologia Clinica ed Elettrostimolazione
Centro Cardiotoracico S. Ambrogio
Indirizzo: Via Luigi Giuseppe Faravelli, 16, 20149 Milano MI
Telefono: 02 331271
Ambulatorio canalopatie/cardiomiopatie
Dipartimento di Scienze Cardio-Toraco
Vascolari e Sanità Pubblica
Azienda Ospedaliera di Padova
Indirizzo: Via Nicolò Giustiniani, 2, 35128 Padova PD
Referente: Dott. Federico Migliore
Telefono: 049 8212321
Email: ambulatorio.cardiologia@aopd.veneto.it
Ambulatorio aritmie e centro per la terapia con dispositivi impiantabili
Policlinico S.Orsola-Malpighi
Indirizzo: Via Giuseppe Massarenti, 9, 40138 Bologna BO
Referente: Dott. Mauro Biffi
Telefono: 051 2143598
Email: pacemaker@aosp.bo.it
Servizio di Aritmologia
Azienda Ospedaliera Universitaria Careggi
Indirizzo: Largo Giovanni Alessandro Brambilla, 3, 50134 Firenze FI
Referente: Dott. Paolo Pieragnoli
Telefono: 055 7946116
UOC Cardiologia e Aritmologia
Dipartimento Cardiochirurgia
Cardiologia e Trapianto Cuore Polmone
IRCCS Ospedale Pediatrico Bambino Gesù
Sede Palidoro
Indirizzo: Via della Torre di Palidoro, 00054 RM
Referente: Prof. Fabrizio Drago
Telefono: 06 68593354
Email: aritmologia@opbg.net
Ambulatorio Aritmologia Cardiologia Vanvitelli
UOSD Diagnostica Aritmologica
Azienda Ospedaliera Monaldi di Napoli
Indirizzo: Via Leonardo Bianchi, 80131 Napoli NA
Referente: Prof. Gerardo Nigro
Telefono: 081 706427
Email: gerardo.nigro@unicampania.it
UOSD Elettrofisiologia, studio e terapia delle aritmie
Azienda Ospedaliera Monaldi di Napoli
Indirizzo: Via Leonardo Bianchi, 80131 Napoli NA
Referente: Dott. Antonio D’Onofrio
Telefono: 0817062605 / 081 7062730 / 081 7065302
Email: antonio.donofrio@ospedalideicolli.it
Servizio di Elettrostimolazione e/o Elettrofisiologia
Policlinico universitario di Bari
Indirizzo: Piazza Giulio Cesare, 70124 Bari BA
Referente: Prof. Stefano Favale
Telefono: 0805592567 / 0805575720
Email: cardiologiauniv@policlinico.ba.it
Servizio di Elettrostimolazione e/o Elettrofisiologia
Azienda Ospedaliera Universitaria Policlinico
“G.Martino” di Messina
Indirizzo: Via Consolare Valeria, 1, 98124 Messina ME
Referente: Dott. Giuseppe Dattilo
Telefono: 090 2213531 / 090 2213061
Ambulatorio controllo pacemaker e Sala CESC
Ospedale Sandro Pertini
Indirizzo: Via dei Monti Tiburtini, 385, 00157 Roma RM
Referente: Dott. Antonello Castro
Telefono: 06 41433434
Email: telecardiologia@aslroma2.it
